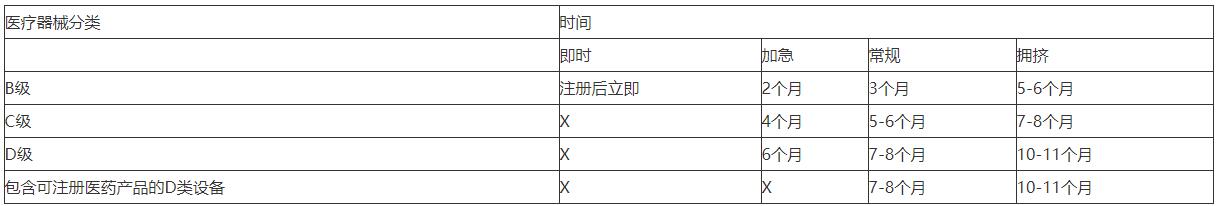
新加坡医疗器械注册流程:
A 类非无菌设备:
A类非无菌医疗器械免于注册,在投放市场前无需向HSA注册。但是,A 类非无菌医疗器械需要在新加坡拥有适当的批发商/进口商许可证的当地代理商。
尽管 A 类非无菌设备不需要在 HSA 注册,但在进入新加坡市场之前,它们仍必须符合医疗器械安全和性能的基本原则。
A 类无菌器械:
第 1 步:通过医疗器械信息和通信系统 (MEDICS)提交申请档案——提交申请后立即收取产品申请费。
第 2 步:审查申请档案 – HSA 进行的审查基于申请人提交的支持数据。如果需要澄清或其他信息,HSA 将向申请人发出请求。
第 3 步:监管决定并在 SMDR 上列出以成功注册 – 在审查提交的申请后,HSA 会做出监管决定。然后,满足注册要求的应用程序将被注册并列在 SMDR 上。
审批时间:1个月
B 类医疗器械:
B类医疗器械的评估途径有4条:
1.全面评估路线——在申请时未获得任何 HSA 参考监管机构的任何事先批准的医疗器械将受全面评估路线的约束。
2.简化评估途径——要获得资格,医疗器械必须至少获得一项监管机构的批准,其标签用途与提交时拟在新加坡营销的用途相同。
3.快速 B 类注册 (EBR) 评估途径
要获得 EBR1 的资格,在提交时,医疗器械必须符合以下标准:
① 获得至少一个 HSA 独立参考监管机构的批准,用于与拟在新加坡营销的用途相同的标签用途。
② 在上述独立参考监管机构的管辖范围内上市至少三年。
③ 在过去三年内,按照产品所有者的预期使用,在全球范围内不存在与医疗器械的使用相关的安全问题。
要获得 EBR2 的资格,医疗器械在提交时必须获得至少两个 HSA 独立参考监管机构的批准,用于标记用途与拟在新加坡营销的用途相同。
4.立即 B 类注册 (IBR) 评估路线
要获得 IBR 评估途径的资格,医疗器械在提交时必须符合以下标准:
① 获得至少两个 HSA 独立参考监管机构的批准,用于与拟在新加坡营销的用途相同的标签用途。
② 在上述两个独立参考监管机构的管辖范围内上市至少三年。
③ 在过去三年内,按照产品所有者的预期使用,在全球范围内不存在与医疗器械的使用相关的安全问题。
④ 任何参考监管机构/该外国司法管辖区或 HSA/新加坡均不会因质量、性能/功效或安全问题而拒绝/撤回医疗器械。
以上评估路线(1-3)的流程:
1.通过 MEDICS 提交申请
2.申请验证
3.申请评估
4.成功注册的监管决定和 SMDR 上市
IBR评估路线的流程:
1.通过 MEDICS 成功提交申请
2.设备已注册并列在 SMDR 上
3.文件验证
C类和D类医疗器械:
C&D类医疗器械的评估途径有3条:
1.全面评估路线(资格定义如上)
2.简略评估路线(资格如上定义)
3.快速评估路线
① 加急 C 类注册 (ECR) –与 EBR 相同的资格
② 快速 D 类注册 (EDR) –要获得 EDR 资格,该设备必须获得至少两个 HSA 独立参考监管机构的批准,用于标记用途与拟在新加坡营销的用途相同。以下设备不符合 EDR:有源植入式设备;与中枢神经系统直接接触的可植入装置;髋关节、膝关节和肩关节置换术;将可注册药物作为辅助作用的设备,用于 HIV 检测或血液/组织供体兼容性检测的 IVD 设备。
上述评估路线(1-3)的流程:
1.通过 MEDICS 提交申请
2.申请验证
3.申请评估
4.成功注册的监管决定和 SMDR 上市